Wie man chemische Verbindungen nennt
Autor:
Laura McKinney
Erstelldatum:
2 April 2021
Aktualisierungsdatum:
26 Juni 2024

Inhalt
- Stufen
- Methode 1 Nomenklatur der ionischen Verbindungen
- Methode 2 Nomenklatur der mehratomigen Verbindungen
- Methode 3 Nomenklatur der kovalenten Verbindungen
Um auf dem Gebiet der Chemie erfolgreich zu sein, muss man wissen, wie man die chemischen Grundverbindungen nennt. In diesem Handbuch finden Sie grundlegende Regeln zum Benennungsprozess für chemische Verbindungen und zum Zuweisen von Namen zu Verbindungen, die Ihnen nicht bekannt sind.
Stufen
Methode 1 Nomenklatur der ionischen Verbindungen
- Was ist eine ionische Verbindung? Ionenverbindungen bestehen aus einem Metall und einem Nichtmetall. Lesen Sie dann im Periodensystem der Elemente nach, welche Kategorien zu den in der Verbindung vorhandenen Elementen gehören.
-

Bilden Sie den Namen. Nichts ist einfacher als die Bezeichnung einer ionischen Verbindung zweier Elemente. In der Tat entspricht der erste Teil des Namens der Verbindung dem Namen des nichtmetallischen Elements mit dem Suffix "ure", während der zweite Teil dem Namen des Metallelements entspricht. Es gibt Ausnahmen: Oxid, Phosphid, Nitrid, Sulfid.- Beispiel: Al2O3. al2 = Aluminium; O3 = Sauerstoff. Der Name der Verbindung lautet also "Aluminiumoxid".
-
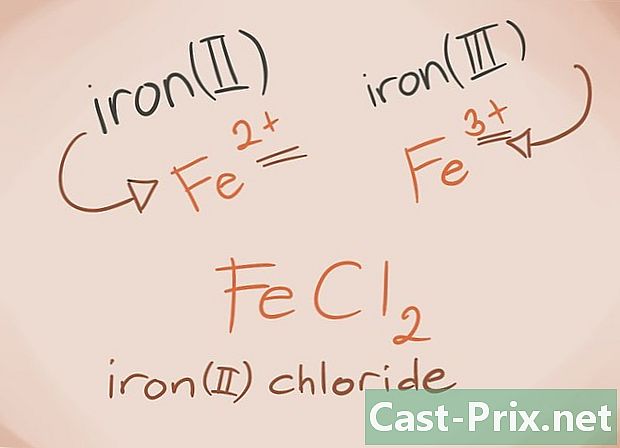
Kennen Sie die Übergangsmetalle Die Übergangsmetalle sind diejenigen, die in den D- und F-Blöcken des Periodensystems gefunden werden. Im Namen der Verbindung ist die Ladung auf diesen Metallen in römischen Ziffern geschrieben. Dies liegt daran, dass Übergangsmetalle mehr Ladung tragen und mehr Verbindungen bilden können.- Beispiel: FeCl2 und FeCl3. Fe = Eisen; Cl2 = -2 Chlorid; Cl3 = Chlorid -3. Als Namen wird es Eisen (II) -chlorid und Eisen (III) -chlorid geben.
Methode 2 Nomenklatur der mehratomigen Verbindungen
-

Sie müssen verstehen, was eine mehratomige Verbindung ist. Polyatomare Verbindungen sind Verbindungen, die durch eine Gruppe von miteinander assoziierten Datomen gebildet werden. Die gesamte Gruppe, die eine Ladung trägt, ist positiv oder negativ. Es gibt dann drei grundlegende Aktionen, die Sie auf mehratomige Verbindungen ausüben können:- Sie können dem ersten Teil der Verbindung einen Wasserstoff hinzufügen. Das Wort "Wasserstoff" wird tatsächlich am Anfang des Namens der Verbindung hinzugefügt. Dies reduziert den Wert der negativen Ladung um eins. Beispielsweise kann das "Carbonat" CO3 wird zum "Hydrogencarbonat" -HCO3.

- Sie können der Verbindung auch Sauerstoff entziehen. Die Last wird nicht geändert, aber das Suffix "-ate" der Verbindung wird in "-ique" geändert. Zum Beispiel die Transformation von: NO3 in NO2 Wir gehen von Nitrat zu Nitrat. "

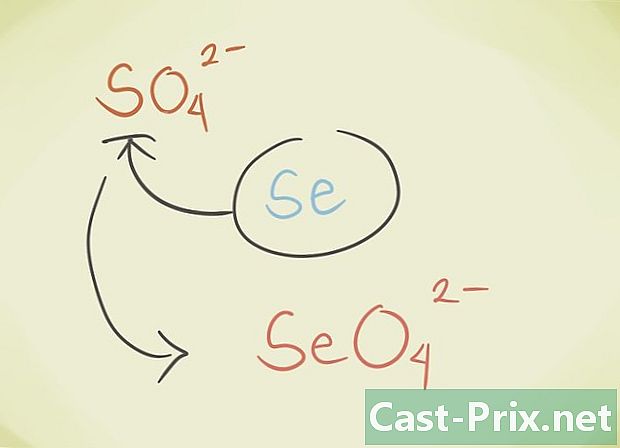
- Sie können das zentrale Latom der Verbindung durch ein anderes Atom der gleichen periodischen Gruppe ersetzen. Zum Beispiel SO-Sulfat4 kann durch Selenat SeO ersetzt werden4.
- Sie können dem ersten Teil der Verbindung einen Wasserstoff hinzufügen. Das Wort "Wasserstoff" wird tatsächlich am Anfang des Namens der Verbindung hinzugefügt. Dies reduziert den Wert der negativen Ladung um eins. Beispielsweise kann das "Carbonat" CO3 wird zum "Hydrogencarbonat" -HCO3.
-

Merken Sie sich die gebräuchlichsten Diongruppen. Die folgenden Gruppen werden zur Bildung der meisten mehratomigen Verbindungen verwendet. In der aufsteigenden Reihenfolge ihrer negativen Ladung haben wir:- Hydroxidionen: OH
- Nitrationen: NO3
- Hydrogencarbonat-Ionen: HCO3
- Permanganationen: MnO4
- Carbonationen: CO3
- Chromationen: CrO4
- Dichromationen: Cr2O7
- Sulfationen: SO4
- Sulfitionen: SO3
- Thiosulfationen: S2O3
- Phosphationen: PO4
- Ammoniumionen: NH4
- Bilden Sie zusammengesetzte Namen aus der obigen Liste. Bilden Sie eine Namensverknüpfung mit den Elementen, die sich auf die Gruppe beziehen. Befindet sich das Element vor der ionischen Gruppe, wird der Elementname einfach an den Anfang des Verbindungsnamens angehängt.
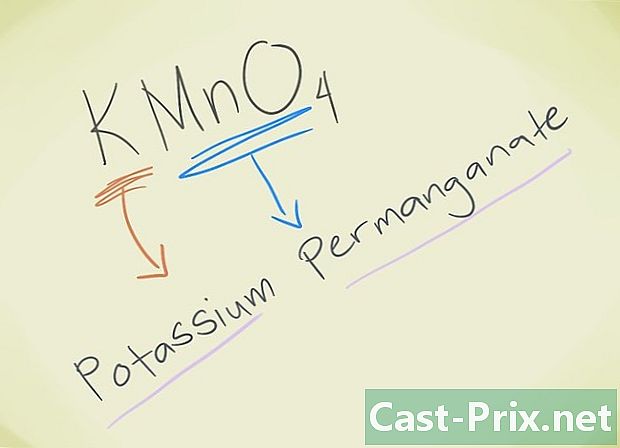
- Beispiel: KMnO4. Sie müssen in der Lage sein, diesen Löwen MnO zu kennen4 entspricht Löwenpermanganat. K bezieht sich auf Kalium. So wird Ihre Verbindung Permanganat-Kalium genannt.
- Beispiel: NaOH. Sie werden hier wahrscheinlich verstanden haben, dass es sich um OHOH handelt. Na ist Natrium, daher wird die Verbindung Natriumhydroxid genannt.

- Beispiel: KMnO4. Sie müssen in der Lage sein, diesen Löwen MnO zu kennen4 entspricht Löwenpermanganat. K bezieht sich auf Kalium. So wird Ihre Verbindung Permanganat-Kalium genannt.
Methode 3 Nomenklatur der kovalenten Verbindungen
-
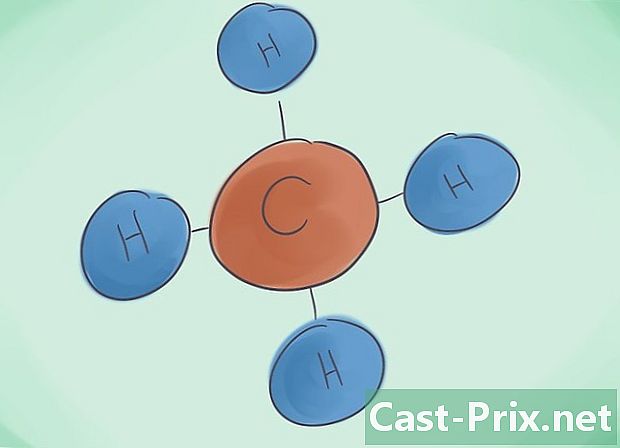
Was ist eine kovalente Verbindung? Die kovalenten Verbindungen resultieren aus der Assoziation von mindestens zwei nichtmetallischen Elementen. Der Name der Verbindung wird durch die Anzahl der Daten bestimmt, aus denen sie besteht. Das griechische Präfix neben diesem Namen gibt die Anzahl der in der Verbindung vorhandenen Moleküle an. -
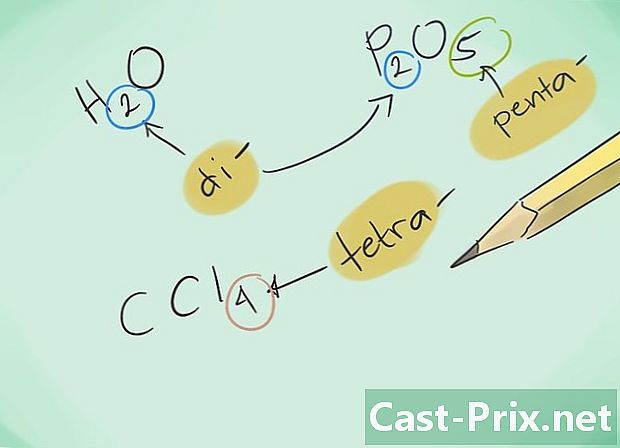
Machen Sie sich mit den Präfixen vertraut. Merken Sie sich die folgenden Präfixe für Verbindungen mit 1 bis 8 Atomen:- 1 Atom - "Mono-"
- 2 Atome - "Di-"
- 3 Atome - "Tri-"
- 4 Atome - "Tetra-"
- 5 Atome - "Penta-"
- 6 Atome - "Hexa-"
- 7 Atome - "Hepta-"
- 8 Atome - "Octa-"
- Nennen Sie dann die Verbindungen. Benennen Sie die resultierende Verbindung mit den entsprechenden Präfixen. Die Präfixe sind auf jedes der Elemente aufzupfropfen, die eine Verbindung mit mehreren Atomen bilden.
- Beispiel: CO kehrt zu Kohlenmonoxid zurück, während CO2 bezeichnet Kohlendioxid.
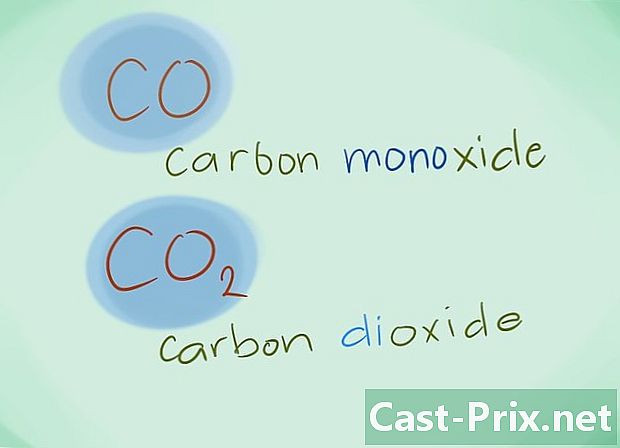
- Beispiel: N2S3 würde salpetrigem Trisulfid entsprechen.

- In den meisten Fällen kann das Präfix "mono" weggelassen werden. Mehr als ein fehlendes Präfix führt dies dazu, dass das letztere verwendet werden sollte. Dieses Präfix wird im Falle von Kohlenmonoxid weiterhin verwendet, da diese Verwendung auf die ersten Schimmer der Chemie zurückgeht.
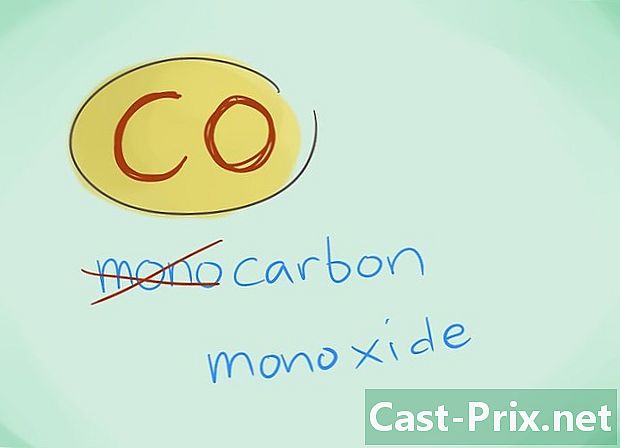
- Beispiel: CO kehrt zu Kohlenmonoxid zurück, während CO2 bezeichnet Kohlendioxid.
- Natürlich vermuten Sie, dass für all diese Regeln mehrere Ausnahmen gelten. Halten Sie zum Beispiel diese Formel, CaCl2Sie erwarten, dass es "Calciumdichlorid" heißt, was NEIN ist. Ihre Verbindung wird einfach den Namen Calciumchlorid behalten.
- Es sollte auch beachtet werden, dass all dies nicht auf die organische Chemie zutrifft.
- Die hier aufgeführten detaillierten Regeln richten sich an ein Anfängerpublikum in Chemie und Naturwissenschaften. Es gibt sehr unterschiedliche Regeln, wenn Sie das Stadium der fortgeschrittenen Chemie durchlaufen, wie die Regeln für die variable Valenz.

